耀海生物,在微生物表達體系領域,擁有豐富的重組蛋白、重組質粒生產服務經驗,聚焦大腸桿菌和酵母菌表達體系,依托GMP級生產車間、完善的質量管理體系,嚴格把控工藝流程,以控制重組生物制品原輔料、中間產物及產物的放行標準,同時保證批間一致性,全面滿足國內外法規要求。
公司可提供GMP級重組蛋白生產服務,涵蓋50L-100L-200L-500L-1000L-2000L多規模發酵平臺,匹配多種規格的低/中/高壓層析系統,以及西林瓶水針/凍干、預充式/卡式瓶全自動無菌灌裝系統。可為客戶提供IND申報樣品生產、I-III期臨床樣品生產、MAH商業化生產服務,全面加速藥物開發進程。

耀海CMO平臺可服務的重組蛋白制品包括:
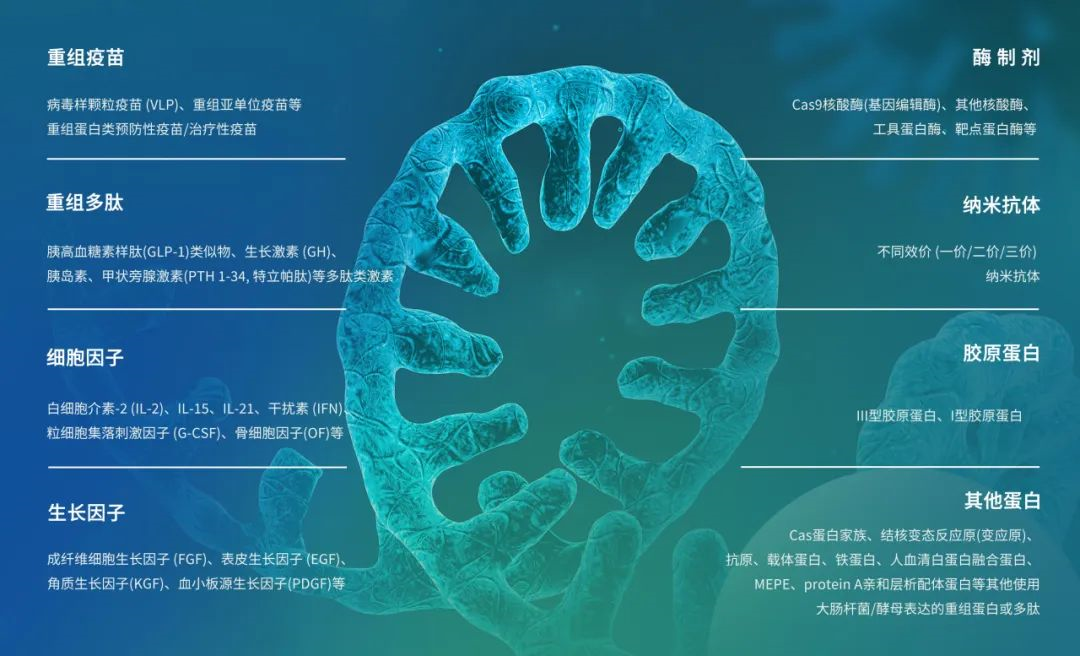
重組蛋白CMO服務詳情
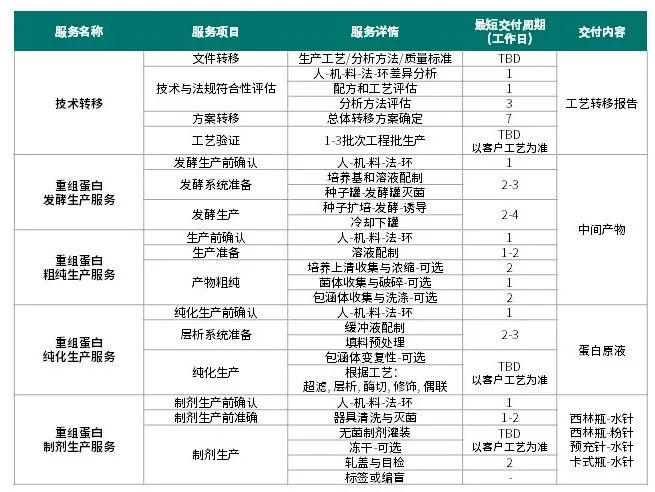
注:所述“重組蛋白”泛指重組蛋白或重組多肽;
TBD: to be determined (以客戶工藝為準)。
多個檢測項目可同時開展。
重組蛋白原液+制劑CMO項目,耀海平均交付周期為3-5個月(含工程批, 周期供參考),實際交付周期以客戶工藝為準。
重組蛋白質量分析與控制服務詳情
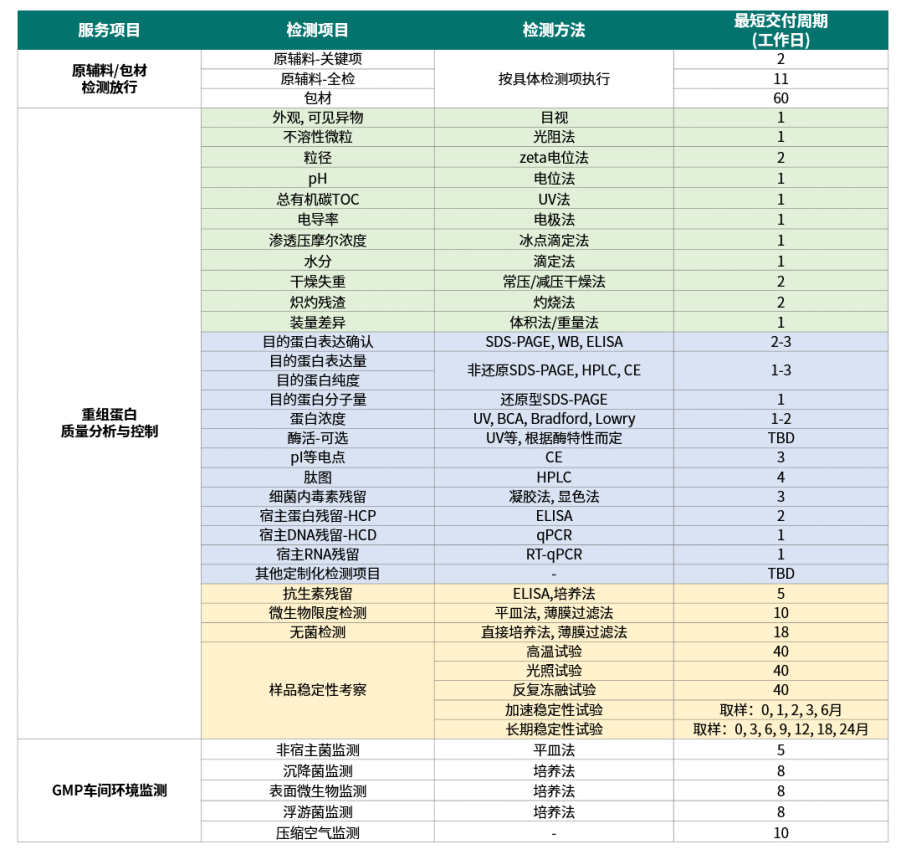
注:所述“重組蛋白”泛指重組蛋白或重組多肽;
TBD: to be determined (以客戶工藝為準)。
多個檢測項目可同時開展。
重組蛋白原液+制劑CMO項目,耀海平均交付周期為3-5個月(含工程批, 周期供參考),實際交付周期以客戶工藝為準。
服務特色
多規模CMO服務平臺
原液車間含GMP級50L-100L-200L-500L-1000L-2000L多規模發酵平臺,匹配對應規模的離心、高壓均質和低壓/高壓層析設備。
制劑車間含GMP級全自動灌裝系統,涵蓋1-25mL西林瓶水針(60,000支/批)和粉針(37,800支/批)、1-3mL預充針/卡式瓶(20,000支/批)。
標準的GMP級防爆車間
防爆配液系統均符合防爆要求,車間安裝靜電釋放儀,并配備可燃氣體報警裝置,可滿足反相層析等特殊工藝配液需求。
合規性保障平臺
全面評估產品及質量標準的合規性,如宿主來源、抗生素類型、毒性或致敏性,滿足注冊申報要求。
質量控制與分析服務
國內外新版藥典和藥品生產指導原則驅動下的質量控制服務,涉及原輔料/包材放行、中間產物放行及產物放行。
豐富的技術轉移/放大經驗
可針對不同規模的發酵和層析系統,調整轉換和放大參數。
截止至目前,已成功交付100+重組蛋白&多肽&質粒CMC項目,其中包括多個IND臨床批件,覆蓋中美雙報及澳洲注冊項目。
開放性線上審計平臺
開放線上審計端口,共享GMP車間VR視頻。